Для понимания сущности гидролиза солей опытным путем определяют их отношение к воде в присутствии индикаторов. Результаты опытов отражены в таблице.

Так как изменение цвета — это признак химической реакции, то можно сделать вывод, что некоторые соли с водой не реагируют, например хлорид натрия, а некоторые реагируют, например хлорид алюминия и карбонат натрия.
Чем это объяснить?
Кроме того, нам известно, что молекула воды хотя и незначительно, но все же диссоциирует на ионы.
С учетом этого рассмотрим данные таблицы о взаимодействии солей с водой.
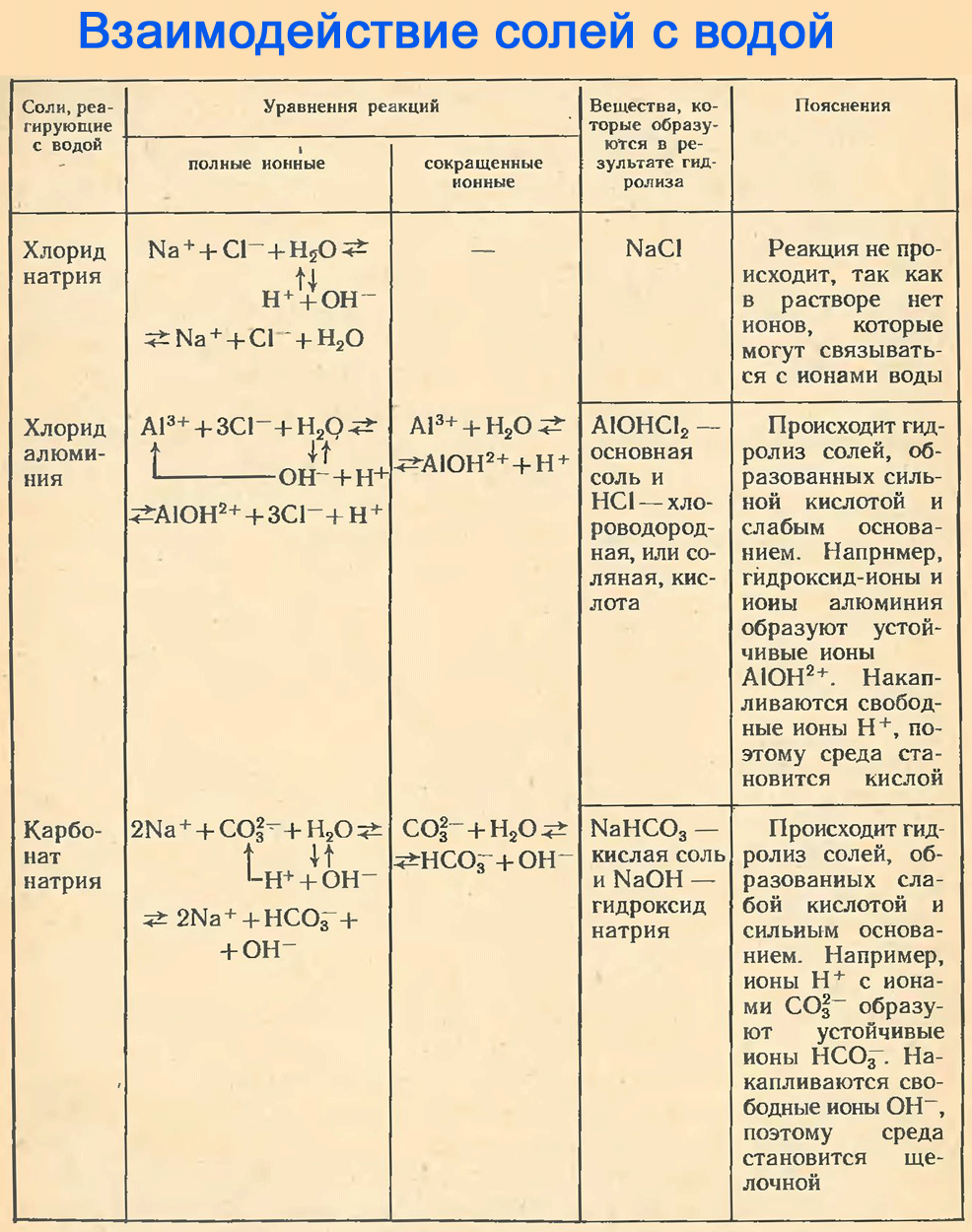
Результаты эксперимента, отраженные в таблице, дают ответ на поставленный выше вопрос:
с водой не реагируют соли, образованные сильным основанием и сильной кислотой, так как ионы таких солей не могут связываться с ионами воды, т. е. ионами Н⁺ и ОН⁻.
Это объясняется тем, что в составе таких солей имеются ионы, которые могут связываться с ионами воды.
Реакции обмена между некоторыми солями и водой относятся к реакциям гидролиза (от греч. «гидро» — вода, «лизис» — разложение).